
 stemintegrado.com
stemintegrado.com
Convierte Patatas o Limones en Electricidad ⚡
Construye una batería con frutas o tubérculos, mide su voltaje y comprende la magia de la electroquímica con un experimento que impresiona en la feria de ciencias.
🎯 Objetivos claros y retadores
- General: Construir y probar una batería casera con patatas o limones para encender un LED o medir voltaje en un multímetro.
- Personal: Optimizar el diseño (tipo de fruta, número de celdas, tamaño de los electrodos) para alcanzar el mayor voltaje estable posible.
🌍 Introducción teórica sencilla y divertida
Una batería transforma energía química en energía eléctrica. En este experimento, la pulpa ácida del limón (o el jugo de la patata) actúa como electrolito. Dos metales diferentes (por ejemplo, zinc y cobre) funcionan como electrodos. Gracias a una reacción de oxidación-reducción, los electrones fluyen del zinc al cobre a través del circuito externo, produciendo una diferencia de potencial (voltaje).
- 🔌 Electrodos: piezas de metal (Zn y Cu) donde ocurren reacciones químicas.
- 💧 Electrolito: medio conductor iónico (ácido cítrico o jugos de la patata).
- ⚡ Voltaje: “empuje” eléctrico; varias celdas en serie suman voltajes.
🔬 Método científico: tu plan de ataque
- Observación: Algunas frutas y tubérculos conducen electricidad.
- Pregunta: ¿Qué combinación (limón vs. patata, tamaño del electrodo, número de celdas) produce más voltaje?
- Hipótesis: Si uso limones frescos y electrodos grandes de Zn y Cu, entonces obtendré mayor voltaje que con patatas.
- Diseño experimental: Mantén constantes la temperatura y el tipo de conexión; cambia solo una variable a la vez.
- Experimentación: Construye celdas y mídeles el voltaje con un multímetro. Anota datos en tablas.
- Análisis: Compara promedios y gráficos; evalúa variabilidad.
- Conclusión: Acepta o refuta la hipótesis y justifica con tus datos.
- Comunicación: Presenta tu póster con esquema, fotos y resultados.
🧩 Descripción gráfica de la maqueta o montaje
Así luce una celda con un limón (o patata). Conecta varias en serie para aumentar el voltaje total.
(+) cable (-)
Cu placa ─────┐ ┌── Zn clavo
│ │
.-''''-. │ │
.' 🍋 '.│ │ LIMÓN (electrolito ácido)
/ Cu Zn \│ │
| || |
\ / │ │
'._ _.' │ │
'---' └──┘
(hacia LED o multímetro)
🛠️ Lista de materiales con opciones inteligentes
| Material | Económica | Estándar | Profesional |
|---|---|---|---|
| Fruta/Tubérculo ácido | 1–4 limones o patatas medianas | 6–8 limones/patatas del mismo tamaño | Docena de limones/patatas calibradas |
| Electrodo de cobre (Cu) | Moneda/cinta de cobre | Placa/lamina de cobre 1–2 cm² | Electrodos de cobre grado laboratorio |
| Electrodo de zinc (Zn) | Clavos galvanizados (zincados) | Tiras de zinc comerciales | Electrodos de zinc puros |
| Cables | Cables con pinza cocodrilo baratos | Set con aislamiento de calidad | Juego banana–cocodrilo apantallado |
| Medición / Carga | LED rojo y resistencia 220–330 Ω | Multímetro digital básico | Multímetro True RMS / data-logger |
| Soporte | Cartón o plastilina | Protoboard pequeño | Placa de montaje con fijaciones |
| Otros | Cinta aislante, marcador | Cinta + cutter + guantes | Kit EPP (gafas, guantes, alfombrilla) |
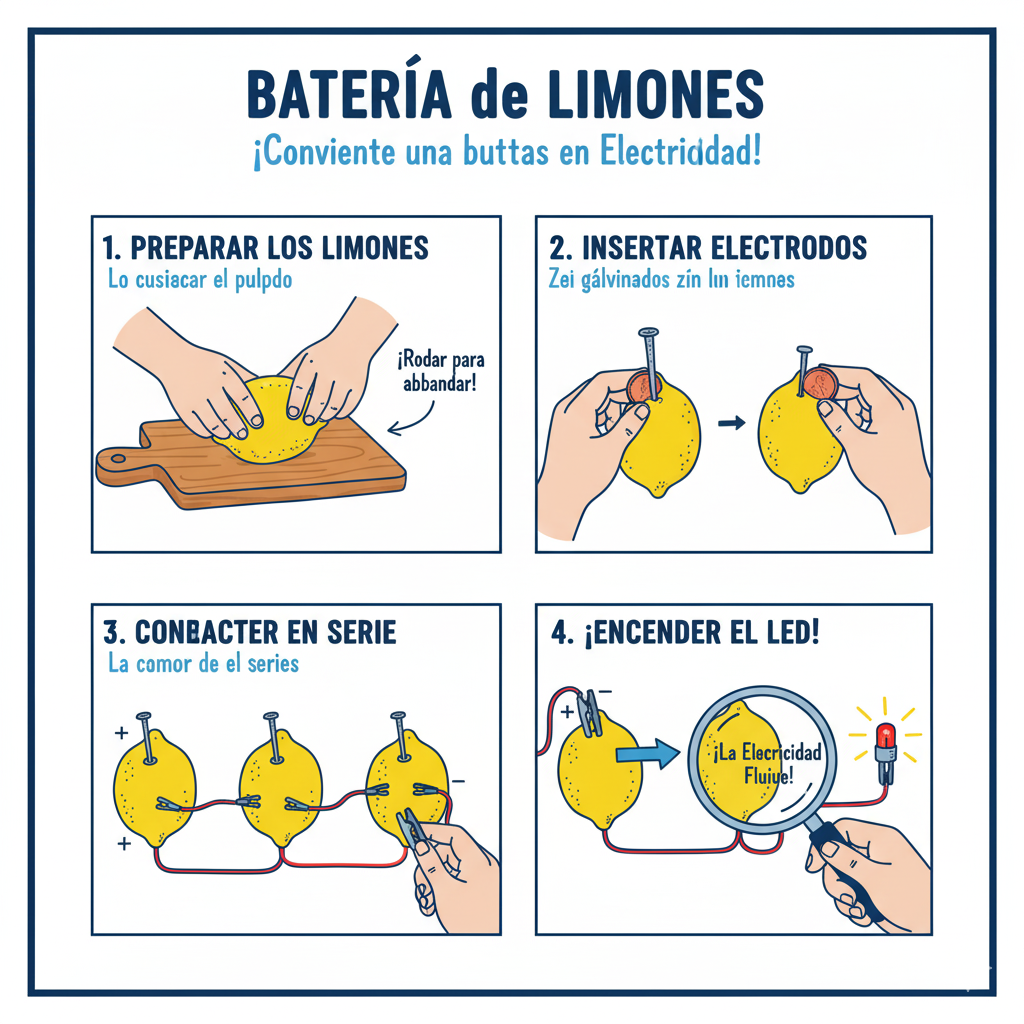
🧭 Guía paso a paso: tu mapa de aventura
1) Prepara las celdas
Rueda suavemente cada limón/patata sobre la mesa para ablandarlo sin romper la piel. Haz dos incisiones pequeñas para insertar cobre y zinc, separadas unos 3–4 cm.
2) Inserta los electrodos
Introduce el electrodo de Zn (clavo galvanizado) y el de Cu (moneda o placa). No deben tocarse dentro de la fruta/tubérculo.
3) Conecta en serie
Une el Cu de la primera celda con el Zn de la segunda, y así sucesivamente. Deja libre un Cu en un extremo y un Zn en el otro para medir el voltaje total.
4) Mide el voltaje
Con un multímetro en modo V DC, coloca la punta roja en el Cu libre (positivo) y la negra en el Zn libre (negativo). Anota el valor en tu hoja de datos.
5) Enciende un LED
Conecta un LED en serie con una resistencia (220–330 Ω). El lado largo del LED va al polo positivo (Cu). Si no enciende, aumenta el número de celdas.
6) Controla variables y repite
Prueba con limón vs. patata, cambia tamaño de electrodos, o agrega más celdas. Registra cada cambio y mide 3 veces para promediar.
🎪 Prepara tu presentación para la feria
- Cartel claro: Título llamativo, foto del montaje, esquema ASCII y diagrama real.
- Interactividad: Permite que el jurado mida el voltaje en vivo o compare limón vs. patata.
- Frases que impresionan: “Nuestra batería es una celda galvánica: el zinc se oxida, el cobre se reduce”.
- Datos clave: Voltaje por celda, número de celdas, resistencia usada, condiciones.
📎 Anexo A — Plantilla de registro de datos
| Prueba | Fruta/Tubérculo | # Celdas | Tamaño electrodos | Voltaje (V) | Comentarios |
|---|---|---|---|---|---|
| 1 | Limón | 4 | Medio | ||
| 2 | Patata | 4 | Medio | ||
| 3 | Limón | 6 | Grande |
✅ Anexo B — Lista de verificación
- Metales (Cu y Zn) limpios
- Conexiones en serie correctas
- LED con resistencia en serie
- Datos anotados con fecha y hora
- Normas de seguridad aplicadas
- Plan para repetir y verificar
🔎 Fuentes recomendadas
Recursos introductorios sobre celdas galvánicas y electroquímica (para ampliar):
- Libro de texto de química general (capítulo de electroquímica).
- Enciclopedias educativas y plataformas de aprendizaje con artículos sobre pilas y baterías.
- Manuales de laboratorio escolar con prácticas de pilas de limón.

